- 628
- 0
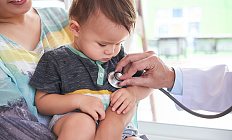
Отеки, боли в ладонях, проблемы с сердцем – как педиатру распознать редкие заболевания
Алгоритмы диагностики и лечения болезни Фабри, мукополисахаридозов и других орфанных патологий.
Невыносимые боли в ладонях и ранний инсульт: чем опасна болезнь Фабри
Болезнь Фабри — редкое генетическое заболевание из группы лизосомных болезней накопления, причиной которого являются мутации в гене GLA, кодирующем фермент альфа-галактозидазу А. Из-за недостатка фермента в клетках начинают накапливаться гликосфинголипиды, что приводит к постепенно нарастающим нарушениям в работе сердца, почек и других органов.
Первые проявления болезни у мальчиков появляются в 6 лет, у девочек — в 9 лет. Однако бывают и исключения. 80% больных с детства жалуются на нейропатические боли на ладонях и подошвах. К другим ранним проявлениям болезни Фабри относятся ангиокератомы — небольшие сосудистые образования на коже, помутнение роговицы, желудочно-кишечные расстройства. У пациентов также часто встречается полное или частичное отсутствие потоотделения (гипогидроз).
Наиболее серьезные осложнения при болезни Фабри начинаются во взрослой жизни. У 25% больных до 30 лет случаются инсульты. В 50% случаев инсульт становится первым клиническим проявлением болезни. Также патология приводит к развитию почечной недостаточности и прогрессирующей кардиомиопатии. 5-8% случаев кардиомиопатии (поражение клапанов, аритмия) приходятся на болезнь Фабри, поэтому детским кардиологам нужно проявлять настороженность и своевременно проверить больного на редкое заболевание.
Фенотипически (по внешним признакам) болезнь Фабри заподозрить очень сложно, однако и тут есть свои характерные особенности. У больных можно увидеть увеличенные скулы, надбровные дуги, выступающую нижнюю челюсть, запавшую переносицу.
В международном регистре по болезни Фабри около пяти тысяч больных из 26 стран. Данные о них собираются в течение 20 лет для оценки существующих препаратов. В России диагностированных пациентов с болезнью Фабри 168 человек, но фактически их может быть гораздо больше.
Для лечения болезни Фабри в нашей стране в настоящее время применяются два зарегистрированных препарата патогенетической терапии: агалсидаза альфа и агалсидаза бета. Первый из них предотвращает прогрессирование болезни Фабри со стороны сердца в течение 20 лет, об этом говорят данные международного исследования, в котором приняли участие 580 пациентов.
К сожалению, часть случаев диагностируется на поздней стадии болезни, что не дает возможность получить значительный эффект от от ферментнозаместительной терапии. Однако на любой стадии болезни начало лечения позволяет замедлить прогрессирование и смягчить клинические проявления.
Деформирует кости и суставы: как заподозрить мукополисахаридоз
Мукополисахаридозы — еще одна группа редких болезней накопления. В результате генетической поломки в хрящах, роговице, сердечных клапанах и зонах роста костей откладываются гликозаминогликаны (ГАГ). Часто родители и сами пациенты отмечают быструю усталость, боли в конечностях, наличие скованности в суставах, нарушения походки и чувствительности тазовых органов и самое угрожающее — отсутствие ходьбы.
Ортопедическими признаками заболевания являются низкий рост, короткие руки и толстые, согнутые пальцы, контрактуры крупных и мелких суставов, карпальный туннельный синдром (наиболее часто встречается у детей с мукополисахаридозом), дисплазия тазобедренной кости, вальгусная деформация коленей.
Диагностировать мукополисахаридоз нужно как можно раньше, но до 18 месяцев сложно провести все диагностические процедуры в силу возраста ребенка. Например, невозможно сделать тест шестиминутной ходьбы. И все же, чем раньше удается выявить заболевание, тем раньше ребенок будет получать лечение, а оно для мукополисахаридозов уже существует. Согласно статистике, средний возраст начала ферментозаместительной терапии при мукополисахаридозе в России — 7-9 лет. Но в некоторых случаях лечение удается начать раньше.
По данным международного исследования, у участников, принимавших препарат ферментозаместительной терапии — идурсульфазу в течение пяти лет, улучшились показатели ГАГ в моче, уменьшился размер печени, увеличилась более чем на 50 метров средняя дистанция шестиминутной ходьбы. При этом наиболее значимые положительные результаты были у детей, лечение которых начали до 18 месяцев.
Болезнь Гоше: ошибки, которых можно избежать
Болезнь Гоше — редкая патология, при которой в селезенке, печени и других органах происходит скопление гликолипидов, хорошо маскируется под видом других тяжелых и смертельно опасных заболеваний. Ее часто путают тромбоцитопенией, анемией, остеомиелитами.
У детей с этим заболеванием болят кости, часто случаются переломы, происходит задержка роста. Чтобы точно установить диагноз, необходимо сдать анализ на активность фермента глюкоцереброзидазы и провести молекулярно-генетическое исследование для подтверждения. Если диагноз подтвердится, ребенку назначается ферментозаместительная терапия. Причем чем раньше ее начать, тем лучше будет качество жизни больного.
«При болезни Гоше ни в коем случае нельзя удалять селезенку, потому что тогда клетки Гоше будут обнаруживаться в печени, легких, в костях — в менее «приспособленных» для этого органах. Удалив селезенку, мы ухудшим прогноз заболевания и качество жизни пациента. Костные кризы нельзя лечить хирургически, хирурги часто рассматривают их как остеомиелиты и начинают антибактериальную терапию. Нужно проводить только консервативную терапию в виде покоя и обезболивания. Гормональная терапия для купирования цитопенического синдрома также противопоказана, и нежелательны препараты железа, потому что анемический синдром у этих пациентом другого генеза»-мнение эксперта.
Смертельные отеки: как врачу не пропустить больного с НАО
Пациенты с наследственным ангионевротическим отеком (НАО) встречаются нечасто, но могут попасть на прием к любому врачу. Идентифицировать это редкое заболевание, напоминающее пищевую и лекарственную аллергическую реакцию, бывает непросто, поэтому в среднем на диагностику НАО в России уходит 17 лет, а пациент проходит около десяти специалистов, хотя в 80% случаев заболевание дебютирует еще до 20 лет. Отеки бывают периферическими — на руках и ногах, а могут быть и намного более опасными — внутренними. Последние в некоторых случаях вызывают непроходимость кишечника и удушье.
По оценкам зарубежных исследователей, без установленного диагноза риск погибнуть у больного с НАО повышается в девять раз. Главная опасность заключается в том, что отеки не отвечают на стандартную антигистаминную терапию.
Пациентов с тяжелыми внутренними отеками нередко отправляют на неоправданные хирургические вмешательства, которых можно избежать. При НАО отек проходит через несколько часов или спустя три-пяти дней. Если отек сохраняется дольше пяти-семи дней, необходимо искать другую причину. В России может быть около 2 тысяч недиагностированных пациентов с НАО. При этом для лечения этой болезни уже существует эффективная лекарственная терапия.
CDKL5-ассоциированное расстройство: ищем среди синдрома Ретта
Долгое время CDKL-5-ассоциированное расстройство считалось атипичной формой синдрома Ретта. Впервые его выявили в 2004 году, но в 2018 идентифицировали как самостоятельную генетическую патологию. Это расстройство возникает в результате мутации гена, отвечающего за выработку фермента, который широко распространен во всех тканях организма, и в особенности в головном мозге. У этого фермента необычная задача: он меняет активность других белков путем добавления к ним атомов кислорода и фосфатной группы для создания или развития нейронных связей.
Ядром всех симптомов у пациентов с мутацией CDKL5 является эпилепсия с ранним дебютом и очень тяжелыми приступами, которая приводит к интеллектуальным нарушениями. Среди других признаков — стереотипии, аутизм, гипервентиляция легких, маленькие стопы и кисти.
Сегодня CDKL5-ассоциированное расстройство признают тяжелой эпилептической энцефалопатией развития с началом в раннем младенчестве. Эпилепсия у этих детей плохо поддается лечению. Только 43% больных могут жить без приступов от 1 до 12 месяцев, у остальных судороги не купируются. Длительная ремиссия возможна у 6% детей. И все же, уже есть новые фармакологические подходы к терапии этого заболевания, которые показали достаточно высокую эффективность.
Задача педиатра— вовремя заподозрить атипичных пациентов среди детей с синдромом Ретта. У последних дебют болезни не бывает таким ранним, как при CDKL5. При синдроме Ретта всегда есть светлый промежуток развития, как правило, он длится до года, а потом начинается регресс и могут присоединяться судороги.
Ссылка: https://dzen.ru/a/ZEkOLkM-Syggz0vC